自家培養角膜上皮「ネピック」:製造販売承認取得のお知らせ
2020.03.19
当社は、「ネピック」の開発を株式会社ジャパン・ティッシュ・エンジニアリング(本社:愛知県蒲郡市、代表取締役 社長執行役員:秋山 雅孝、以下「J-TEC」)に委託し、J-TEC が「ネピック」の製造販売承認を取得しました。「ネピック」は、角膜上皮幹細胞疲弊症(※1)の治療を目的としたもので、眼科領域で国内初の再生医療等製品です。
今回、製造販売承認を取得した「ネピック」は、患者自身の角膜輪部組織から角膜上皮幹細胞を採取してシート状に培養したもので、本品を移植することにより角膜上皮を再建させることを目的としています。

当社は、J-TEC と協力し、再生医療等製品の開発を加速させるとともに、再生医療の実用化・産業化を進め、患者の生活の質(QOL)の向上へも寄与することを目指します。
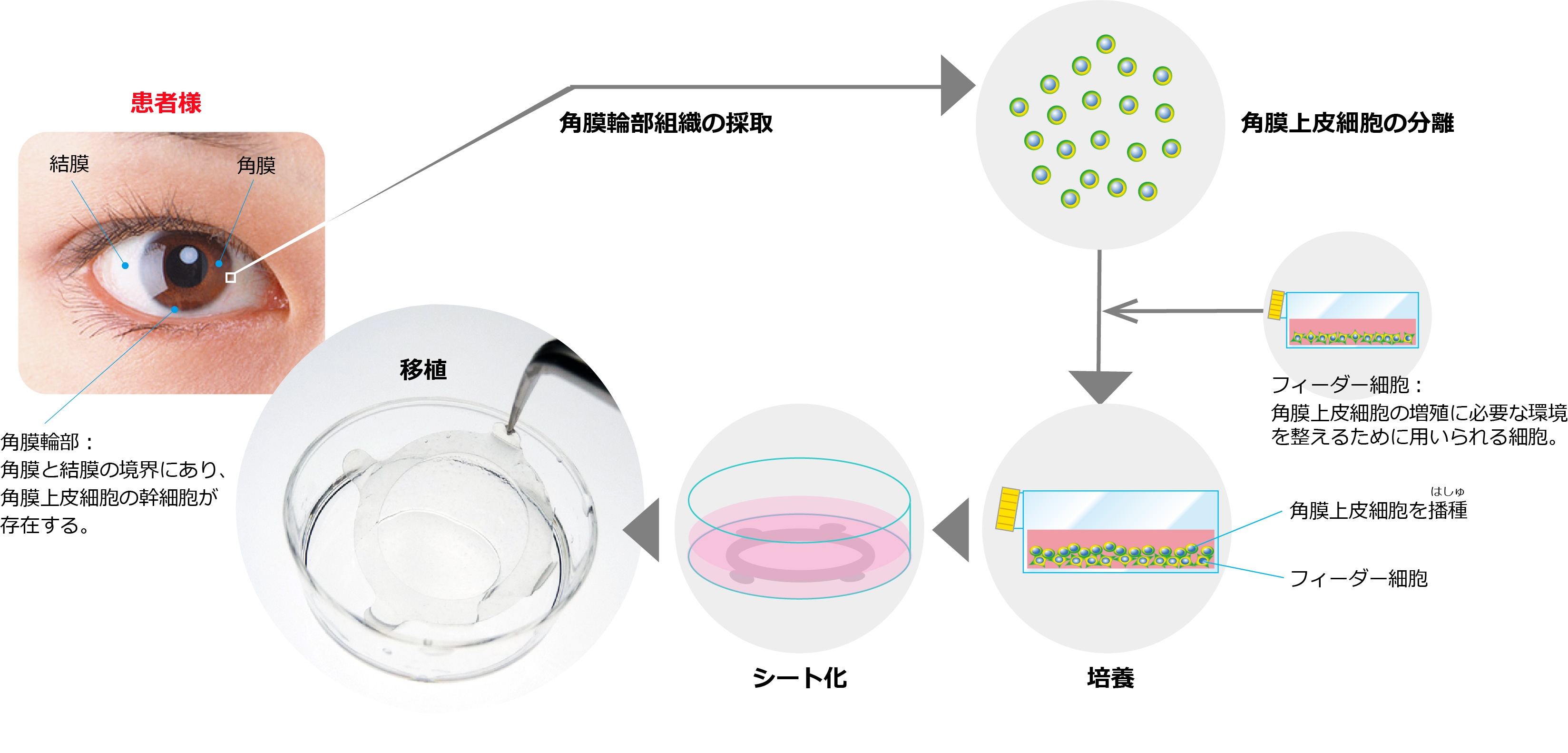
※1 角膜上皮幹細胞疲弊症
結膜と角膜の境界領域である角膜輪部に存在する角膜上皮幹細胞が、先天的または外的要因等によって消失することで発症する疾患。角膜が混濁し、視力の低下や、眼痛などの臨床症状が見られます。
製造販売承認の概要
製造販売承認の概要は以下のとおりです。
| 承認番号 | 30200FZX00002000 |
|---|---|
| 承認年月日 | 2020年3月19日 |
| 一般的名称 | ヒト(自己)角膜輪部由来角膜上皮細胞シート |
| 販売名 | ネピック |
| 効能、効果又は性能 | 角膜上皮幹細胞疲弊症。ただし、以下の患者を除く。 ・スティーヴンス・ジョンソン症候群の患者 ・眼類天疱瘡の患者 ・移植片対宿主病の患者 ・無虹彩症等の先天的に角膜上皮幹細胞に形成異常を来す疾患の患者 ・再発翼状片の患者 ・特発性の角膜上皮幹細胞疲弊症患者 |
| 承認条件 | 1.角膜上皮幹細胞疲弊症に関連する十分な知識及び経験を有する医師が、本品の使用方法に関する技能や手技に伴う合併症等の知識を十分に習得した上で、角膜上皮幹細胞疲弊症の治療に係る体制が整った医療機関において「効能、効果又は性能」並びに「用法及び用量又は使用方法」を遵守して本品を用いるよう、関連学会との協力により作成された適正使用指針の周知、講習の実施等、必要な措置を講ずること。
2.治験症例が極めて限られていることから、原則として再審査期間が終了するまでの間、全症例を対象に使用の成績に関する調査を実施することにより、本品使用患者の背景情報を把握するとともに、本品の安全性及び有効性に関するデータを早期に収集し、本品の適正使用に必要な措置を講ずること。 3.本品の製造過程にフィーダー細胞として用いられているマウス胎児由来3T3-J2細胞にかかる異種移植に伴うリスクを踏まえ、最終製品のサンプル及び使用に関する記録を30 年間保存するなど適切な取扱いが行われるよう必要な措置を講ずること。 |
一覧へ戻る





























 TOP
TOP